発電設備
燃料電池

燃料電池とは
電気化学反応で水素と酸素から電気を直接取り出し!!
中学校でも行われる有名な実験である水の電気分解の逆の反応になります
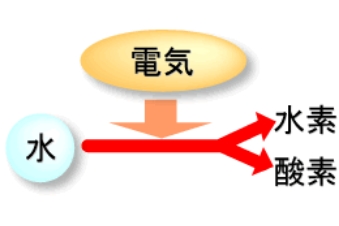
発電の原理<水の電気分解>
参考)水の電気分解とは、水に白金や黒鉛などの電極を入れて電流を流すと、水(H2O)が分解されて水素と酸素が発生するというものです。
燃料電池の発電方法
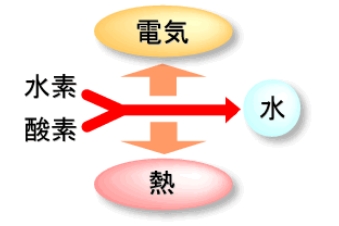
燃料電池は、水の電気分解の逆のプロセスを利用した装置です。水素と酸素の化学反応によって水を生成すると同時に、その過程で発生する電気を取り出します。
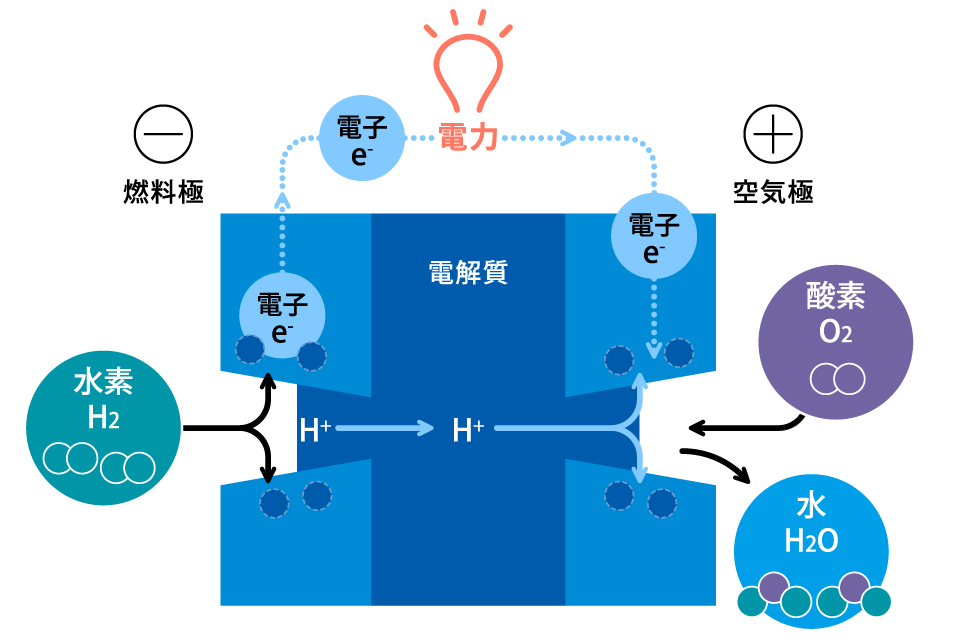
燃料極では、水素燃料を供給することで、触媒反応によって水素イオン(H+)と電子(e-)が生成されます。燃料電池に用いられる電解質は、イオンは通すものの電子は通さないため、水素イオン(H+)は電解質を通過して空気極へ移動します。一方、電子(e-)は電解質に妨げられて直接通過できないため、外部の回路を通して移動させ、その際に電気として取り出されます。
空気極では、酸素が供給され、触媒反応によって酸素分子(O₂)が酸素原子に分離します。この酸素原子に、外部回路を通って移動してきた電子(e-)と電解質を通じて運ばれてきた水素イオン(H+)が結合することで、水(H₂O)が生成されます。これにより、二酸化炭素(CO₂)を生成・排出することなく発電が可能となります。
燃料電池の特長
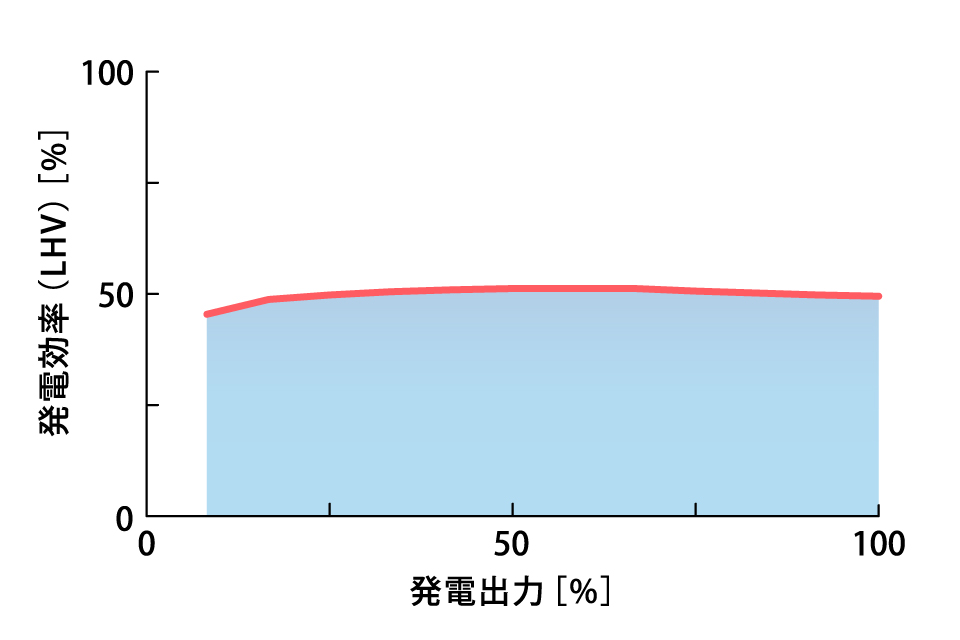
さらに、燃料電池は水素燃料が持つエネルギーを熱や動力を介さず直接電気へと変換する仕組みを採用しているため、幅広い発電出力範囲(8%~100%)において、安定して高い発電効率を実現できます。この特性により、燃料電池は低出力から高出力まで効率よく運転することが可能であり、さまざまな利用環境に対応できます。
燃料電池の原理
効率グラフ(例)
水素燃料電池システム
連携企業との協創体制により、水素供給などの課題にも柔軟に対応








